Introduction :
Dans les articles précédents , nous avons abordé la corrosion galvanique et la corrosion électrolytique par courant de fuite continu.
Reste un autre problème, plus mal connu et encore controversé : la corrosion électrolytique en courant alternatif.
Il existe même une école de pensée qui va jusqu’à nier le phénomène en théorisant que les ions métalliques arrachés au métal pendant une alternance vont revenir se plaquer pendant l’alternance de signe opposé, pour une perte finale de masse nulle.
Bien que cette théorie apparaisse raisonnable et séduisante, elle s’avère fausse : l’eau de mer contient quantité d’ions négatifs qui vont se combiner avec les ions métalliques positifs et les empêcher de revenir se déposer, avec pour conséquence une corrosion de la pièce.
Théorie et Expérimentation :
Un expert américain (Dick Troberg, Professional Boatbuilder n° 105 fév/mars 2007), travaillant pour des compagnies d’assurances, a mené une série d’expériences afin d’essayer d’y voir plus clair.
- Dans une première expérience, deux échantillons d’alliage léger dans un bac d’eau de mer ont été soumis :
- A un courant de 600 mA sous 14 V alternatif : les deux échantillons ont été dissous en 30 mn
- A un courant de 600 mA sous 14 V continu : l’échantillon relié au + a été dissous en 10 mn.
Ceci montre que la théorie des optimistes semble se vérifier partiellement, mais que la corrosion en alternatif existe bel et bien.
Ce qui rend le problème inquiétant est que les tensions en alternatif (230 V ou 115 V) sont beaucoup plus élevées qu’en continu, d’où des courants de fuite en proportion. Or l’effet de l’électrolyse est proportionnel à l’intensité : le risque est donc grand de dégâts catastrophiques et rapides.
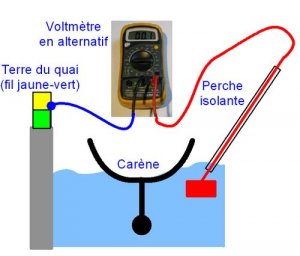
- Afin d’évaluer la susceptibilité relative des matériaux courants, il a ensuite mené une série d’expériences suivant le schéma ci-contre :
- Un échantillon de 3 mm de diamètre et 3 mm de long est relié au réseau, l’autre fil étant relié à une plaque d’aluminium, le tout étant immergé dans l’eau de mer. Le critère retenu est le temps jusqu’à la coupure électrique de l’échantillon.
- Les résultats (en minutes) sont schématisés sur le graphe ci-après : ils sont pour le moins surprenants !
- Que peut-on en conclure :
- Une première remarque importante est que le zinc et l’aluminium ont permuté leur positions par rapport au tableau d’électropositivité classique : en alternatif l’alu protège le zinc !
- La seconde remarque est la position du fer qui est moins affecté que les autres métaux, apparemment du fait de la création d’une couche d’oxyde protectrice.
Ces phénomènes, même s’ils sont mal expliqués, sont néanmoins extrêmement préoccupants et demandent donc une surveillance attentive.
En pratique comment faire sur nos bateaux :
- Il existe des testeurs de courant de fuite permettant la détection de très faibles courants de fuite alternatifs, de l’ordre de 0,01 mA (Fluke 360, Chauvin Arnoux F62….). Malheureusement ces appareils coûtent entre 400 et 700 €.
- Faire une mesure d’isolation entre votre circuit bord et la masse bateau est une bonne idée, mais il vaut mieux utiliser pour cela un contrôleur d’isolation que votre multimètre : la tension de mesure est trop faible pour avoir un résultat crédible. 500 à 1 000 V de tension d’essai sont préférables si les problèmes viennent d’isolants défectueux ou humides.
- Lors des tests, à faire de préférence circuit par circuit, s’assurer que l’équipement consommateur est réellement en fonctionnement : un piège classique est le thermoplongeur du chauffe-eau, souvent élément à problème, qui n’est connecté par le thermostat que si l’eau est froide… : vider l’eau chaude avant la mesure !
- Un transformateur d’isolation est une bonne sécurité, mais ne protège pas des courants alternatifs baladeurs dans l’eau du port, par exemple entre bateaux voisins de votre place.
En complément à cet article, on pourra lire sur le site :
La corrosion galvanique : 1- le bateau isolé
La corrosion galvanique : 2- le bateau dans son environnement
La corrosion électrolytique par courant de fuite continu
La corrosion électrolytique par courant de fuite alternatif
Mesures de contrôle en protection galvanique


 Suivi RSS
Suivi RSS Conception
Conception


 Version imprimable
Version imprimable Publié Juillet 2011, (màj Mai 2019) par :
Publié Juillet 2011, (màj Mai 2019) par :